Lorsque vous découvrez qu’un médicament n’est pas disponible dans votre pays, cela peut sembler être une impasse ou la fin de la route.
Dans bien des cas, ce n’est pas le cas.
Si un traitement a été approuvé dans un autre pays ou est encore en cours de développement, les patients pourraient être en mesure d’y accéder par des voies légales avant qu’il ne devienne disponible localement.
Ces canaux sont des moyens valides pour les patients d’obtenir des médicaments qui ne sont pas encore disponibles localement.
Ce guide explique ce que signifie l’accès anticipé, les options légales disponibles et ce que les patients doivent savoir avant d’envisager l’accès transfrontalier aux médicaments.
Qu’est-ce que l’accès précoce aux médicaments ?
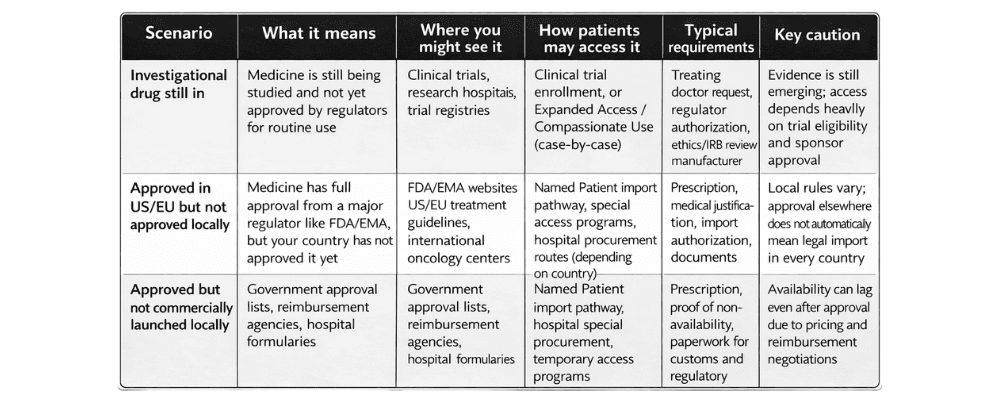
« Accès anticipé » désigne des programmes réglementés qui permettent aux patients de recevoir des médicaments en dehors de la chaîne d’approvisionnement commerciale standard lorsque :
- Le médicament est approuvé dans un autre pays mais n’est pas encore disponible localement.
- Le médicament est toujours en cours d’examen par les régulateurs.
- Le patient souffre d’une affection grave ou potentiellement mortelle, avec peu d’options de traitement.
Différents pays utilisent des termes différents, mais les mécanismes courants incluent :
- Programmes d’accès élargi (EAP)
- Programmes d’utilisation compassionnelle
- Voies d’importation des patients nommées
Ces programmes sont conçus pour les patients qui ont hâte d’être disponibles régulièrement sur le marché.
À qui sont généralement destinés les programmes en accès anticipé
Maladie rare : Un patient atteint d’une maladie génétique rare pourrait découvrir qu’une thérapie ciblée est disponible dans une autre région, mais pas encore fournie localement. S’il n’existe pas d’alternatives efficaces, un médecin peut explorer des méthodes réglementées pour demander l’accès à ce patient spécifique.
Oncologie : Un patient atteint d’un cancer avancé peut avoir un biomarqueur tumoral qui correspond à une thérapie ciblée nouvellement approuvée aux États-Unis ou en UE, mais le médicament n’est pas encore disponible dans les hôpitaux locaux. Dans certains cas, un médecin peut envisager des options d’accès précoce tout en s’assurant que le processus est conforme aux réglementations nationales.
Maladie potentiellement mortelle : Pour les conditions à progression rapide ou potentiellement mortelles où l’attente peut aggraver considérablement les résultats, les médecins évaluent parfois les options d’accès précoce lorsque les traitements standards ont échoué ou ne sont pas appropriés, et que le profil bénéfice-risque soutient l’accès.
Lorsque le temps presse, la question n’est pas seulement de savoir ce qui existe à l’échelle mondiale, mais aussi ce qui est légalement possible pour un patient spécifique sous supervision médicale en ce moment.
Accès élargi (États-Unis)
Aux États-Unis, la FDA régule l’accès élargi, parfois appelé usage compatissant, par le biais de règles formelles. Ces règles permettent aux patients atteints de maladies graves de recevoir des médicaments expérimentaux en dehors des essais cliniques.
Points clés :
- Le médecin traitant doit déterminer qu’il n’existe pas d’alternative comparable
- Le bénéfice potentiel doit justifier les risques potentiels
- Le fabricant doit accepter de fournir le médicament
- La FDA doit autoriser l’accès
- Un comité d’examen institutionnel (IRB) doit examiner la demande
Usage compatissant (Union européenne)
Dans l’Union européenne, les programmes d’utilisation compassionnelle offrent l’accès à des médicaments non approuvés pour les patients atteints de maladies chroniques, graves ou potentiellement mortelles lorsqu’aucune thérapie autorisée satisfaisante n’est disponible.
Ces programmes sont coordonnés au niveau national mais encadrés par l’Agence européenne des médicaments (EMA).
Chaque pays de l’UE met en œuvre ses propres procédures dans ce cadre.
Voies d’importation des patients nommées
De nombreux pays autorisent les médecins à demander des médicaments non approuvés ou non commercialisés localement pour chaque patient, via ce qu’on appelle souvent la voie du patient nommé.
Bien que les règles varient selon les pays, les éléments communs incluent :
- Une ordonnance valide d’un médecin agréé
- Confirmation que le médicament n’est pas disponible localement
- Documentation attestant que le médicament est destiné à un usage personnel
- Formulaires réglementaires exigés par le pays d’origine
- Respect des lois douanières et d’importation pharmaceutique
Ces systèmes sont utilisés par les hôpitaux et les médecins du monde entier et sont réglementés par les autorités sanitaires nationales.
Mythe vs Fait : Comprendre l’importance de la médecine légale
Mythe : L’importation de médicaments est une activité du marché noir
Fait : Des voies légales d’accès précoce existent dans de nombreux pays. Lorsqu’elle est réalisée par des canaux réglementaires appropriés, sous la supervision des médecins et en conformité avec les exigences de documentation, l’importation de médicaments peut être légale et réglementée.
Mythe : Il faut attendre l’approbation locale
Fait : Dans de nombreuses régions, l’accès peut être possible une fois qu’un médicament est approuvé par une autorité de régulation reconnue, telle que la FDA ou l’EMA, même si l’approbation locale est encore en attente. L’éligibilité spécifique dépend des lois nationales.
Mythe : Une ordonnance suffit à vous
Fait : Une ordonnance n’est généralement que le point de départ. La documentation supplémentaire inclut souvent :
- Formulaires de déclaration du patient
- Applications réglementaires
- Documents d’autorisation d’importation
- Documentation douanière
- Dans certains cas, des lettres de justification du médecin
Les documents manquants peuvent entraîner des retards ou un refus.
Pourquoi le timing est important
Il peut falloir plusieurs années avant qu’un médicament nouvellement approuvé soit disponible à la vente dans tous les pays. Les délais d’examen réglementaire, les négociations tarifaires et les processus de remboursement peuvent varier considérablement.
Bien que les systèmes réglementaires travaillent en étroite mesure pour garantir la sécurité et la qualité, une maladie grave peut amener les patients à attendre des années pour un traitement.
Cependant, toute décision de poursuivre l’accès anticipé doit être la suivante :
- Sur recommandation médicale
- Évalué pour rapport au risque par rapport au bénéfice
- Conduite strictement dans le cadre légal
L’attente devrait être une décision médicale, pas seulement une issue bureaucratique.
Exemple de chronologie :
Un médicament contre le cancer approuvé par la FDA en 2024 peut encore mettre de 2 à 5 ans avant d’être largement disponible dans un autre pays en raison d’étapes supplémentaires, notamment la révision réglementaire locale, les négociations de prix, les décisions de remboursement et l’intégration de la chaîne d’approvisionnement.
Pendant cette période, certains patients peuvent bénéficier d’options d’accès anticipé réglementées, selon les règles locales.
Ce que les patients doivent faire en premier
Si on vous dit qu’un traitement n’est pas disponible localement :
- Confirmez si le médicament est approuvé ailleurs
- Demandez à votre médecin si les programmes d’accès anticipé s’appliquent
- Vérifiez si votre pays dispose d’un patient nommé ou d’une voie similaire
- Comprendre les exigences de documentation
- Confirmez que la pharmacie ou le fournisseur d’origine respecte les lois sur l’exportation
Les patients ne devraient jamais acheter de médicaments sur ordonnance auprès de sources en ligne non vérifiées qui prétendent contourner les réglementations.
L’Organisation mondiale de la santé met en garde contre les risques posés par les médicaments falsifiés et de qualité inférieure dans les marchés non réglementés.
Considérations de conformité et de sécurité
L’accès légal anticipé doit toujours inclure :
- Supervision médicale
- Approvisionnement vérifié du fabricant
- Transport à température contrôlée lorsque nécessaire
- Déclaration douanière appropriée
- Documentation réglementaire
- Suivi clair de la pharmacovigilance
L’accès transfrontalier aux médicaments doit respecter les réglementations pharmaceutiques des pays exportateurs et importateurs.
Une perspective équilibrée
Des voies d’accès précoce existent pour soutenir les patients atteints de maladies graves dont les options sont limitées. Ils sont des mécanismes structurés, réglementés et légalement reconnus.
Cependant :
- Tous les médicaments ne sont pas éligibles
- Tous les pays n’autorisent pas les importations de la même manière
- Tous les patients ne remplissent pas les critères d’éligibilité
- La participation du fabricant peut être requise
Les patients méritent une transparence tant sur les possibilités que sur les limites.
Dernière réflexion
« Non disponible localement » ne signifie pas toujours « n’existe pas ». Cela peut signifier que l’approbation n’est pas encore arrivée dans votre pays.
Des voies légales d’accès précoce comme les programmes d’accès élargi, d’utilisation compassionnelle et de patients nommés existent pour combler cet écart. Lorsqu’elles sont utilisées correctement sous la supervision d’un médecin et en pleine conformité avec les exigences réglementaires, elles peuvent être bénéfiques.
Si vous envisagez cette voie, commencez par une discussion médicale. Vérifiez la réglementation de votre pays et assurez-vous que chaque étape respecte les procédures légales appropriées.
Les décisions de santé doivent être informées, conformes et guidées par des professionnels, en particulier lorsqu’elles concernent des médicaments transfrontaliers.
Références
Food and Drug Administration des États-Unis. Accès élargi.
Agence européenne des médicaments. Usage compatissant.
Agence de régulation des médicaments et produits de santé du Royaume-Uni. Fourniture de produits médicinaux non autorisés (Specials).
Organisation mondiale de la santé. Des produits médicaux de mauvaise qualité et contrefaits.
Guide connexe
Directives d’importation de médicaments d’Espagne pour usage personnel
Directives d’importation de médicaments d’Australie pour usage personnel
Directives d’importation de médicaments du Canada pour usage personnel
Directives d’importation de médicaments de la Grèce pour usage personnel
Directives d’importation de médicaments des Pays-Bas pour un usage personnel
Directives d’importation de médicaments d’Allemagne pour usage personnel






