自分の国で医薬品が入手できないと分かったとき、行き止まり、あるいは道の終わりのように感じるかもしれません。
多くの場合、そうではありません。
治療法が他国で承認されているか、まだ開発中である場合、患者は国内で利用可能になる前に合法的な手段でアクセスできる可能性があります。
これらのチャネルは、患者が現地でまだ入手できない医薬品を入手するための有効な手段です。
このガイドでは、早期アクセスの意味、利用可能な法的選択肢、国境を越えた医薬品へのアクセスを検討する前に患者が知っておくべきことについて説明します。
医薬品の早期アクセスとは何ですか?
「早期アクセス」とは、以下の場合に患者が標準的な商業サプライチェーン外で医薬品を受け取ることを許可する規制対象プログラムを指します。
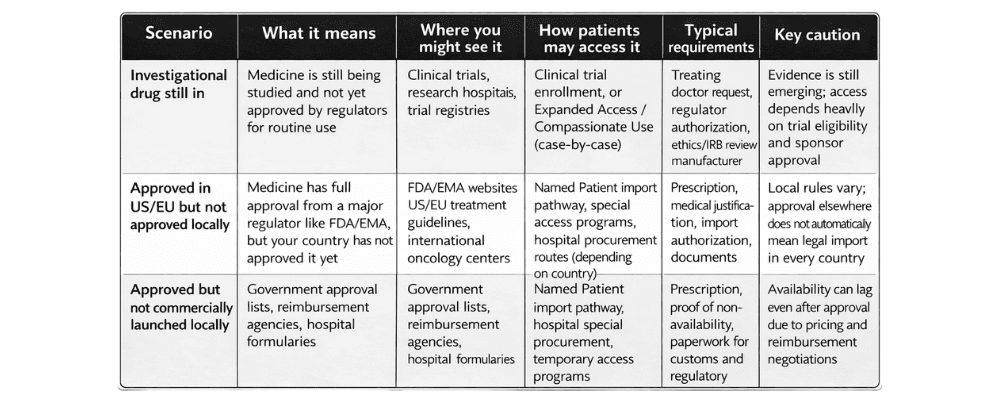
- この薬は他国では承認されているが、国内ではまだ入手できない。
- この薬はまだ規制当局による審査中だ。
- 患者は治療の選択肢がほとんどない重篤なまたは生命を脅かす状態にあります。
国によって用語は異なりますが、一般的なメカニズムは次のとおりです。
- 拡大アクセスプログラム(EAP)
- 慈悲使用プログラム
- 指定患者輸入経路
これらのプログラムは、通常の市場での入手を待つことができない患者向けに設計されています。
早期アクセスプログラムは通常誰を対象としているのか
希少疾患:希少な遺伝性疾患を持つ患者は、他の地域では利用可能な標的治療法があるものの、地元ではまだ提供されていないことに気づくかもしれません。効果的な代替手段がない場合、医師は特定の患者へのアクセスを申請するための規制された方法を検討する場合があります。
腫瘍学:進行がんの患者が、米国またはEUで新たに承認された標的治療と一致する腫瘍バイオマーカーを有しているものの、その薬剤がまだ現地の病院で入手できない場合があります。場合によっては、医師は、国の規制に準拠した手続きを踏んでいることを確認しながら、早期アクセスの選択肢を検討することがあります。
生命を脅かす病気: 待機すると結果が大幅に悪化する可能性がある、急速に進行する、または生命を脅かす病気の場合、標準的な治療が失敗したか適切でなく、ベネフィット リスク プロファイルがアクセスをサポートするときに、医師は早期アクセス オプションを評価することがあります。
時間が重要な場合、問題は世界的に何が存在するかだけではなく、特定の患者に対して医師の監督下で現在何が法的に可能なのかということである。
拡大アクセス(米国)
米国では、FDA(米国食品医薬品局)が正式な規則を通じて、拡大アクセス(コンパッショネートユースとも呼ばれる)を規制しています。この規則により、重篤な疾患を持つ患者は臨床試験以外で治験薬を投与されることができます。
要点:
- 担当医は同等の代替手段が存在しないと判断する必要がある
- 潜在的な利益は潜在的なリスクを正当化しなければならない
- 製造業者は薬剤の提供に同意しなければならない
- FDAはアクセスを許可する必要がある
- 機関審査委員会(IRB)が申請を審査する必要がある
人道的使用(欧州連合)
欧州連合では、慢性疾患、重篤疾患、または生命を脅かす疾患を患う患者に対し、認可された満足のいく治療法がない場合に、人道的使用プログラムによって未承認の医薬品へのアクセスが提供されます。
これらのプログラムは国家レベルで調整されていますが、欧州医薬品庁 (EMA) によって指導されています。
各 EU 加盟国は、この枠組みに基づいて独自の手続きを実施します。
指定患者輸入経路
多くの国では、いわゆる「指定患者経路」を通じて、医師が個々の患者に対して未承認の医薬品や現地で販売されていない医薬品を要求することが認められています。
ルールは国によって異なりますが、共通の要素は次のとおりです。
- 資格のある医師からの有効な処方箋
- 現地でその薬が入手できないことの確認
- 薬が個人使用であることを記載した文書
- 輸入国で必要な規制フォーム
- 税関および医薬品輸入法の遵守
これらのシステムは世界中の病院や医師によって使用されており、各国の保健当局によって規制されています。
神話と事実:合法医薬品の輸入を理解する
誤解:医薬品の輸入は闇市場活動である
事実:多くの国で合法的な早期アクセスの道筋が存在します。適切な規制当局の手続きを経て、医師の監督下で、必要な書類を揃えて輸入すれば、医薬品の輸入は合法かつ規制の対象となります。
誤解:地方自治体の承認を待たなければならない
事実:多くの地域では、FDAやEMAなどの公認規制当局による承認が得られれば、たとえ現地での承認がまだ保留中であっても、医薬品へのアクセスが可能になる場合があります。具体的な資格要件は各国の法律によって異なります。
誤解:処方箋だけで十分
事実:処方箋は通常、出発点に過ぎません。多くの場合、追加書類として以下のものが含まれます。
- 患者申告書
- 規制アプリケーション
- 輸入許可書類
- 税関書類
- 場合によっては医師の正当化の手紙
書類が不足していると、遅延や拒否が発生する可能性があります。
タイミングが重要な理由
新たに承認された医薬品がすべての国で販売されるまでには、数年かかる場合があります。規制当局による審査のスケジュール、価格交渉、償還プロセスは国によって大きく異なります。
規制システムは安全性と品質を確保するために慎重に機能していますが、重篤な病気の場合、患者は治療に何年も待たされる可能性があります。
ただし、早期アクセスを追求するかどうかの決定は、次の条件を満たす必要があります。
- 医師のアドバイスに基づいて
- リスクとベネフィットを評価
- 法的枠組み内で厳密に実施
待つことは単なる官僚的な結果ではなく、医学的な決定であるべきです。
タイムラインの例:
2024 年に FDA によって承認されたがん治療薬が、現地の規制当局による審査、価格交渉、償還決定、サプライ チェーンのオンボーディングなどの追加手順があるため、他国で広く利用できるようになるまでには、さらに 2 ~ 5 年かかる可能性があります。
このギャップの間、一部の患者は地域の規則に応じて、規制された早期アクセス オプションの対象となる場合があります。
患者が最初にすべきこと
地元では治療を受けられないと言われた場合:
- その薬が他国で承認されているかどうかを確認する
- 早期アクセスプログラムが適用されるかどうか医師に確認してください
- あなたの国に指定患者制度または類似の制度があるかどうかを確認してください
- ドキュメント要件を理解する
- 供給元の薬局またはサプライヤーが輸出法を遵守していることを確認する
患者は、規制を回避すると主張する未検証のオンラインソースから処方薬を決して購入してはなりません。
世界保健機関は、規制されていない市場で偽造医薬品や粗悪医薬品がもたらすリスクについて警告している。
コンプライアンスと安全性に関する考慮事項
法的早期アクセスには常に次の内容が含まれます。
- 医師の監督
- 検証済みのメーカー調達
- 必要に応じて温度管理された配送
- 適切な税関申告
- 規制文書
- 明確な医薬品安全性監視追跡
国境を越えた医薬品へのアクセスは、輸出国と輸入国の両方の医薬品規制に準拠する必要があります。
バランスのとれた視点
早期アクセスパスウェイは、選択肢が限られている重篤な疾患の患者を支援するために存在します。これらは構造化され、規制され、法的に認められたメカニズムです。
しかし:
- すべての薬が適格なわけではない
- すべての国が同じように輸入を許可しているわけではない
- すべての患者が適格基準を満たすわけではない
- メーカーの参加が必要になる場合があります
患者は可能性と限界の両方について透明性を得る権利がある。
最終的な考え
「現地では入手できません」は必ずしも「存在しない」という意味ではありません。お住まいの国でまだ承認されていない可能性があります。
このギャップを埋めるために、拡大アクセス、コンパッショネートユース、ネームド・ペイシェント・プログラムといった法的な早期アクセス経路が存在します。医師の指導の下、規制要件を完全に遵守して適切に利用すれば、これらのプログラムは有益となり得ます。
この方法を検討している場合は、まず医師に相談してください。お住まいの国の規制を確認し、すべての手順が適切な法的手続きに従っていることを確認してください。
健康に関する決定は、特に国境を越えた医薬品に関わる場合には、専門家による十分な情報に基づいた、規則に従った、指導の下で行われるべきです。
参考文献
米国食品医薬品局。拡大アクセス。
欧州医薬品庁。人道的使用。
英国医薬品・医療製品規制庁。未承認医薬品(スペシャル)の供給。
世界保健機関。基準を満たさない偽造医薬品。





