Когда вы узнаёте, что лекарство недоступно в вашей стране, это может показаться тупиком или концом пути.
Во многих случаях это не так.
Если лечение одобрено в другой стране или всё ещё разрабатывается, пациенты могут получить к нему доступ через легальные каналы до того, как оно станет доступным локально.
Эти каналы являются эффективными способами для пациентов получить лекарства, которые ещё не доступны в регионе.
В этом руководстве объясняется, что такое ранний доступ, какие легальные варианты доступны и что пациентам следует знать перед тем, как рассматривать трансграничный доступ к медицине.
Что такое ранний доступ к лекарствам?
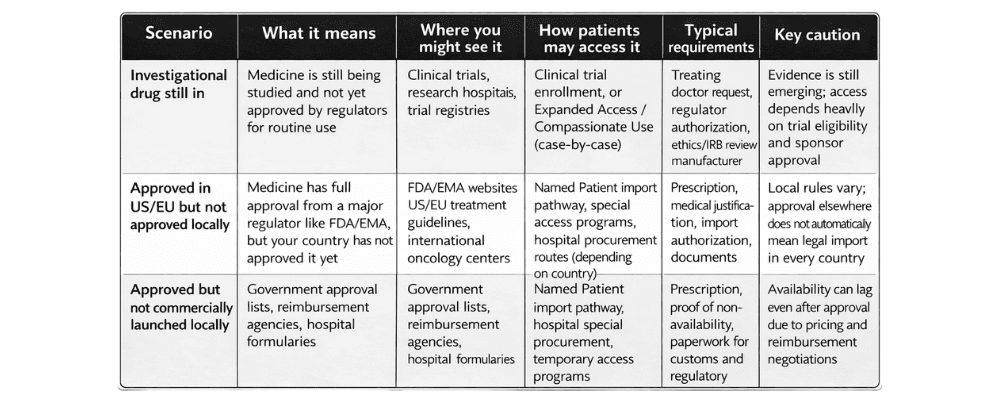
«Ранний доступ» относится к регулируемым программам, позволяющим пациентам получать лекарства вне стандартной коммерческой цепочки поставок, когда:
- Лекарство одобрено в другой стране, но пока не доступно в регионе.
- Лекарство всё ещё находится на рассмотрении регуляторами.
- У пациента серьёзное или угрожающее жизни заболевание и мало вариантов лечения.
В разных странах используются разные термины, но распространённые механизмы включают:
- Программы расширенного доступа (EAP)
- Программы сострадательного использования
- Именованные пути импорта пациентов
Эти программы предназначены для пациентов, которые не могут дождаться регулярной доступности на рынке.
Для кого обычно предназначены программы раннего доступа
Редкое заболевание: Пациент с редким генетическим заболеванием может обнаружить, что таргетная терапия доступна в другом регионе, но пока не предоставляется локально. Если эффективных альтернатив нет, врач может рассмотреть регулируемые методы запроса доступа для конкретного пациента.
Онкология: У пациента с запущенным раком может быть биомаркер опухоли, соответствующий недавно одобренной таргетной терапии в США или ЕС, но лекарство пока не доступно в местных больницах. В некоторых случаях врач может рассмотреть варианты раннего доступа, обеспечивая соответствие процесса национальным нормам.
Угрожающее жизни заболевания: при быстро прогрессирующих или угрожающих жизни состояниях, где ожидание может значительно ухудшить исходы, врачи иногда оценивают варианты раннего доступа, если стандартные методы лечения не дают результатов или не подходят, а профиль выгоды и риска поддерживает доступ.
Когда время критически важно, вопрос заключается не только в том, что существует в мире, но и в том, что юридически возможно для конкретного пациента прямо сейчас под медицинским наблюдением.
Расширенный доступ (США)
В Соединённых Штатах FDA регулирует расширенный доступ, иногда называемый сострадательным использованием, формальными правилами. Эти правила позволяют пациентам с серьёзными заболеваниями получать исследовательские препараты вне клинических испытаний.
Ключевые моменты:
- Лечащий врач должен определить, что аналогичной альтернативы не существует
- Потенциальная выгода должна оправдывать потенциальные риски
- Производитель должен согласиться предоставить препарат
- FDA должно разрешить доступ
- Институциональный ревизионный совет (IRB) должен рассмотреть запрос
Сострадательное использование (Европейский союз)
В Европейском союзе программы сострадательного использования предоставляют доступ к неодобренным лекарствам для пациентов с хроническими, серьёзными или угрожающими жизни заболеваниями, когда нет удовлетворительных разрешённых методов терапии.
Эти программы координируются на национальном уровне, но управляются Европейским агентством по лекарственным средствам (EMA).
Каждая страна ЕС реализует свои собственные процедуры в рамках этой структуры.
Именованные пути импорта пациентов
Во многих странах врачи разрешают запрашивать неодобренные или не продаваемые на рынке лекарства для отдельных пациентов через так называемый «Именованный пациентский путь».
Хотя правила различаются в зависимости от страны, распространённые элементы включают:
- Действительный рецепт от лицензированного врача
- Подтверждение, что лекарство недоступно в регионе
- Документы, подтверждающие, что лекарство предназначено для личного пользования
- Регуляторные формы, требуемые страной-импортером
- Соблюдение таможенного и фармацевтического законодательства
Эти системы используются больницами и врачами по всему миру и регулируются национальными органами здравоохранения.
Миф против факта: понимание импорта легальных лекарств
Миф: Импорт лекарств — это деятельность на чёрном рынке
Факт: легальные пути раннего доступа существуют во многих странах. Если это осуществляется через надлежащие регуляторные каналы, под наблюдением врача и в соответствии с требованиями документации, импорт лекарств может быть легальным и регулируемым.
Миф: Нужно дождаться местного одобрения
Факт: во многих регионах доступ к препарату может быть возможен после одобрения признанного регулирующего органа, такого как FDA или EMA, даже если местное одобрение ещё ожидается. Конкретное право на участие зависит от национальных законов.
Миф: Рецепт — это всё, что нужно
Факт: Рецепт обычно является только отправной точкой. Дополнительная документация часто включает:
- Формы декларации пациентов
- Регуляторные применения
- Документы на разрешение на импорт
- Таможенная документация
- В некоторых случаях письма с обоснованием врача
Отсутствие документов может привести к задержкам или отказу.
Почему важно время
Может потребоваться несколько лет, прежде чем новый одобренный препарат станет доступен для продажи в каждой стране. Сроки регуляторного обзора, переговоры по ценообразованию и процессы возмещения расходов могут сильно различаться.
Хотя регуляторные системы работают тщательно для обеспечения безопасности и качества, серьёзные заболевания могут заставить пациентов ждать лечение годами.
Однако любое решение о раннем доступе должно быть следующим:
- На основе медицинских рекомендаций
- Оценка по риску и выгоде
- Проводится строго в рамках правовых рамок
Ожидание должно быть медицинским решением, а не просто бюрократическим решением.
Пример хронологии:
Лекарство от рака, одобренное FDA в 2024 году, может потребоваться от 2 до 5 лет, чтобы стать широко доступным в другой стране благодаря дополнительным шагам, включая местный регуляторный обзор, переговоры по ценообразованию, решения о возмещении расходов и внедрение цепочки поставок.
В этот период некоторые пациенты могут претендовать на регулируемые варианты раннего доступа, в зависимости от местных правил.
Что пациентам следует сделать в первую очередь
Если вам говорят, что лечение недоступно локально:
- Проверьте, одобрено ли лекарство в других местах
- Спросите у врача, применяются ли программы раннего доступа
- Проверьте, есть ли в вашей стране Именованный пациент или похожий путь
- Понимание требований к документации
- Убедитесь, что исходная аптека или поставщик соответствует экспортным нормам
Пациентам никогда не следует покупать рецептурные лекарства у непроверенных онлайн-источников, которые утверждают, что обходят правила.
Всемирная организация здравоохранения предупреждает о рисках, связанных с фальсифицированными и некачественными лекарствами на нерегулируемых рынках.
Вопросы соответствия и безопасности
Юридический ранний доступ всегда должен включать:
- Надзор врача
- Проверено происхождение производителя
- Доставка с контролируемой температурой при необходимости
- Правильная таможенная декларация
- Нормативная документация
- Четкое отслеживание фармаковигиланса
Трансграничный доступ к лекарствам должен соответствовать фармацевтическим нормам как экспортирующих, так и импортеров.
Сбалансированная перспектива
Существуют пути раннего доступа для поддержки пациентов с серьёзными заболеваниями, у которых ограниченные варианты. Это структурированные, регулируемые и юридически признанные механизмы.
Однако:
- Не каждое лекарство подходит под это
- Не во всех странах импорт разрешен одинаково
- Не каждый пациент соответствует критериям соответствия
- Может потребоваться участие производителя
Пациенты заслуживают прозрачности как возможностей, так и ограничений.
Заключительная мысль
«Недоступно локально» не всегда означает «не существует». Это может означать, что одобрение ещё не пришло в вашу страну.
Существуют легальные пути раннего доступа, такие как Расширенный доступ, Сострадательное использование и программы Именованных Пациентов, чтобы преодолеть этот разрыв. При правильном использовании под руководством врача и в полном соответствии с нормативными требованиями они могут быть полезны.
Если вы рассматриваете этот путь, начните с медицинского обсуждения. Проверяйте нормативные акты вашей страны и следите за всеми необходимыми юридическими процедурами.
Решения о здоровье должны приниматься информированно, соблюдаться и направляться профессионалами, особенно когда речь идёт о лекарствах за границами.
Ссылки
Управление по контролю за продуктами и лекарствами США. Расширенный доступ.
Европейское агентство по лекарственным средствам. Сострадательное использование.
Агентство по регулированию лекарственных средств и медицинских товаров Великобритании. Поставка нелицензированных лекарственных средств (Specials).
Всемирная организация здравоохранения. Некачественные и поддельные медицинские продукты.
Связанное руководство
Руководящие принципы по импорту лекарств Испании для личного пользования
Руководящие принципы по импорту лекарств Австралии для личного пользования
Руководящие принципы Канады по импорту лекарств для личного пользования
Рекомендации по импорту лекарств в Греции для личного пользования
Руководящие принципы по импорту лекарств в Нидерландах для личного пользования
Руководящие принципы по импорту лекарств в Германии для личного пользования






